新闻动态
2025 SGO·中国之声|LBA重磅公布BRIGHT研究,生物标志物指引下替雷利珠单抗联合方案,助力铂耐药卵巢癌新突破
发布时间:2025-03-26 11:00 浏览:13755次
2025年3月14-17日,第56届美国妇科肿瘤学年会(SGO 2025)在西雅图盛大召开。作为全球范围内最权威的妇科肿瘤学术会议之一,众多期待已久的重磅研究成果纷纷亮相,为卵巢癌等妇科肿瘤临床诊疗带来了新方法、新视角。其中,华中科技大学同济医学院附属同济医院马丁院士、高庆蕾教授团队牵头的一项生物标志物驱动的靶向治疗铂耐药复发卵巢癌(PROC)的BRIGHT研究在本次大会的焦点论坛(Focused Forum)中惊艳亮相,为通过精准诊疗改善PROC患者预后提供了新启示。

1、PROC患者预后不佳,亟需探索更精准、有效的治疗方案
卵巢癌是最致命的妇科恶性肿瘤。由于其发病隐匿,超过70%的卵巢癌在确诊时已处于晚期,此时肿瘤已经扩散并形成了复杂的肿瘤内异质性。铂类化疗仍然是卵巢癌全身治疗的基石。尽管患者对初始化疗反应良好,但80%的卵巢癌患者最终会复发。其中约20%~30%的患者在完成最后一次化疗后的6个月内复发,从而被诊断为PROC。PROC患者的预后极差,治疗选择有限。而且,非铂类单药化疗对PROC的疗效有限。利用生物标志物驱动的前沿疗法联合治疗方案对于改善PROC的预后至关重要。
在卵巢癌患者中,约15%~20%携带体系或胚系BRCA1/2突变(BRCAm),多种PARP抑制剂可通过合成致死机制使这部分患者获益。其中,帕米帕利是一种高效、选择性的口服PARP1/2抑制剂,且不是P-糖蛋白或乳腺癌耐药蛋白的底物,从而避免了其他PARP抑制剂中常见的耐药机制。帕米帕利在BRCAm患者中显示出持久的抗肿瘤活性和可管理的安全性,尤其是在PROC患者中。但在占大多数的BRCA1/2野生型(BRCAwt)患者中,PROC管理更具挑战性,其接受PARP抑制剂治疗的获益相对有限。值得期待的是,ANNIE等研究提示,PARP抑制剂联合抗血管生成药物在PROC治疗中具有良好的抗肿瘤活性,有望成为PROC患者的一种潜在治疗选择。
免疫检查点抑制剂(ICI)已改变了多种癌症的治疗模式,并为PROC的治疗提供了新的机会。然而,不幸的是,卵巢癌仍是少数几种从ICI中获益有限且目前尚无适应证获批的癌症之一。优化患者选择可能最大化治疗获益,但在PROC中长期缺乏有效的ICI治疗生物标志物。近期有研究显示,缺乏免疫原性T细胞浸润与PROC中ICI疗效受损相关。在多种癌症中,高水平的CD8+肿瘤浸润淋巴细胞(TILs)可以预测ICI单药治疗或基于ICI的联合治疗的疗效,这表明,具有足够预先存在的CD8+TILs的患者可能对ICI有更好的反应。然而,预先存在的CD8+TILs水平是否能够预测PROC患者中ICI的疗效尚不清楚,仍需进一步研究来验证这一假设。
令人欣喜的是,本次SGO大会公布的BRIGHT研究结果证实了基于生物标志物(BRCA突变状态结合CD8+TILs状态)的靶向治疗在PROC患者中的潜在临床获益,为临床精准治疗带来宝贵参考。
2、BRIGHT研究结果重磅公布,BRCA/CD8+TIL有望指导PROC精准靶向治疗
BRIGHT研究(NCT05044871)是一项开放标签、多中心、Ⅱ期伞式试验,旨在评估基于生物标志物的靶向联合治疗方案(包括PARP抑制剂帕米帕利、PD-1抑制剂替雷利珠单抗、贝伐珠单抗和白蛋白结合型紫杉醇)在PROC患者中的疗效和安全性。该研究共纳入108例PROC患者(定义为最后一次铂类化疗后6个月内疾病进展),并根据BRCA突变状态和CD8+TILs计数分配治疗方案。组1纳入BRCA突变(BRCAm)患者,接受帕米帕利+贝伐珠单抗治疗(N=30);组2纳入BRCA野生型(BRCAwt)肿瘤且CD8+TILs阳性(≥3)的患者,接受替雷利珠单抗+贝伐珠单抗+白蛋白结合型紫杉醇治疗(N=72);组3纳入BRCAwt且CD8+ TILs
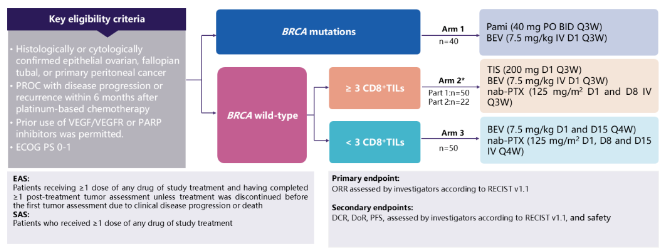
从入组患者基线特征来看,BRCAwt且CD8+TILs≥3的患者占大多数。患者均经过多线治疗,且基线肿瘤负荷较高。具体而言,组1、组2和组3患者的中位年龄分别为55.0岁、55.5岁和60.0岁;高级别浆液性卵巢癌患者的比例分别为96.7%、84.7%和66.7%;既往接受过≥2线系统治疗患者比例分别为93.3%、70.8%和83.3%,且大量患者接受过≥4线治疗(60.0%、34.7%和50.0%)。值得注意的是,在三个治疗组中,最后一次治疗到疾病进展时间≤3个月的患者比例分别高达63.3%、52.8%和66.7%,使用过PARP抑制剂治疗的患者占比为40.0%、47.2%和16.7%,既往经治的铂耐药患者占比为73.3%、65.3%、50.0%。

研究结果显示,截至数据截止日期(2024年11月28日),组1、组2和组3的中位随访时间分别为11.1个月、12.3个月和12.2个月,三组患者的ORR分别为28.6%、48.6%和50.0%。组2达到了基于贝叶斯预测概率预设的疗效边界,第1部分和第2部分的合并ORR为48.6%(95% CI 36.4-60.8)。
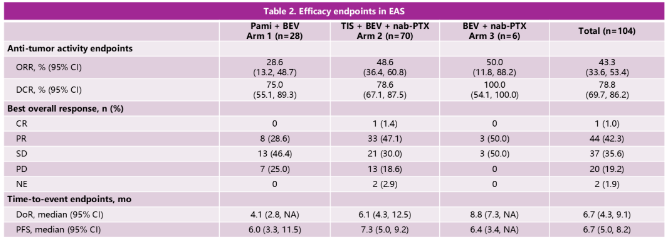
此外,对组2患者进行亚组分析发现,无论既往是否使用过PARP抑制剂(使用过 vs 未使用过:55.9% vs 41.7%)、VEGF/VEGFR抑制剂(50.0% vs 46.4%)和白蛋白结合型紫杉醇(46.8% vs 52.2%),均不影响ORR;而CD8+ TILs计数可能与ORR相关,CD8+ TILs≥10患者的ORR达到57.1%,在数值上高于CD8+ TILs计数≥3~
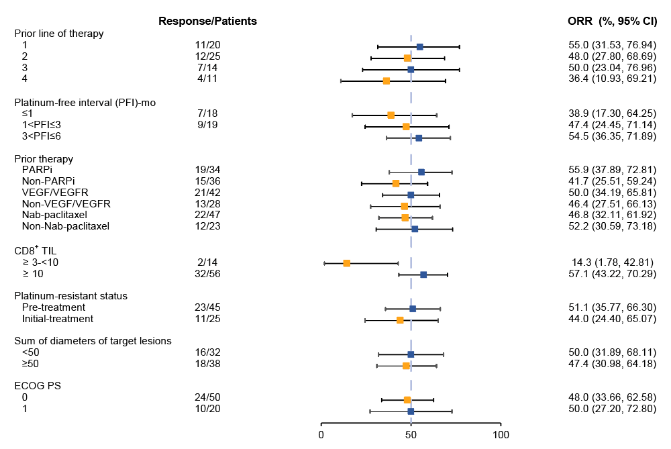
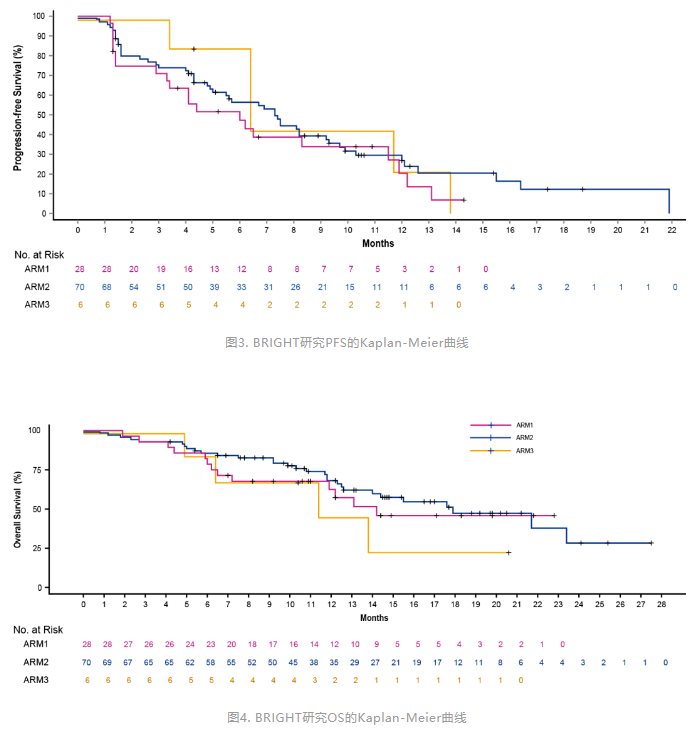
在生存结局方面,中位随访11.4个月时,组1、组2和组3的中位PFS分别为6.0个月、7.3个月和6.4个月;中位总生存期(OS)分别为14.2个月、17.9个月和11.4个月。
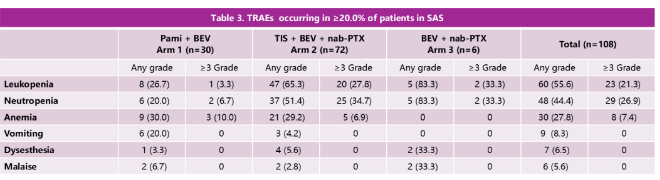
此外,在三组患者中,联合治疗方案的总体耐受性良好。组1、组2和组3中≥3级治疗相关不良事件(TRAEs)的发生率分别为30.0%、55.6%和33.3%;严重不良事件(SAEs)的发生率分别为23.3%、31.9%和16.7%。在组2中,16例(22.2%)发生了任意级别的免疫相关不良事件(irAEs),其中5例(6.9%)为≥3级。由此可见,替雷利珠单抗+贝伐珠单抗+白蛋白结合型紫杉醇联合治疗的安全性可控。
综上所述,BRIGHT研究结果表明,对于临床中常见的BRCAwt且CD8+ TILs≥3的患者,尽管其既往接受过多线治疗且基线肿瘤负荷高,但基于PD-1抑制剂的联合治疗方案(替雷利珠单抗+贝伐珠单抗+白蛋白结合型紫杉醇)仍取得了显著的疗效,ORR达48.6%,中位PFS达7.3个月,中位OS高达17.9个月,并具有可耐受的安全性特征。同时,帕米帕利+贝伐珠单抗治疗BRCAm患者以及贝伐珠单抗+白蛋白结合型紫杉醇治疗BRCAwt且CD8+ TILs
3、新进展层出不穷,点燃PROC治疗新希望
PROC是卵巢癌治疗中的一大难题,其预后差、治疗选择有限,长期以来一直是临床研究的重点。尤其是随着PARP抑制剂、ICI、抗体药物偶联物(ADC)等新型疗法的不断涌现,PROC的治疗格局正在发生深刻变化。近年来,随着对肿瘤耐药机制理解的加深,基于ICI的免疫联合治疗方案已成为临床探索的重点,并在PROC治疗中展现出巨大的应用潜力。例如,PARP抑制剂可利用DNA修复机制的缺陷,通过一系列分子和细胞机制调节肿瘤免疫微环境,增强抗肿瘤免疫反应并增强ICI的疗效。在TOPACIO研究中,尼拉帕利联合帕博珠单抗治疗PROC患者的ORR为18%。此外,免疫联合抗血管生成药物治疗PROC患者也具有一定疗效。一项国内II期研究中,PD-1抑制剂联合抗血管生成药物治疗37例PROC患者,中位PFS为4.1个月,中位OS为18.9个月,ORR为24.3%,疾病控制率(DCR)为54.1%。另一项II期研究中,免疫治疗、化疗及抗血管生成药物联合治疗PROC患者的ORR达43.3%,中位PFS为7.6个月。而在BRIGHT研究组2中,替雷利珠单抗+贝伐珠单抗+白蛋白结合型紫杉醇在接受过多线治疗且肿瘤负荷高的PROC患者中依然取得了令人满意的疗效和安全性,ORR达48.6%,中位PFS达7.3个月,中位OS达17.9个月,充分展现了该联合疗法在BRCAwt且CD8+ TILs≥3的PROC患者中的广阔应用前景。
ADC作为当前临床研究的热点,也在PROC治疗领域进行了积极探索。例如,针对叶酸受体α(FRα)的ADC药物索米妥昔单抗(MIRV)在FRα高表达PROC患者中显示出显著疗效。MIRASOL研究中,MIRV单药治疗组的ORR达42.3%,中位PFS为5.62个月,中位OS为16.46个月,≥3级AEs、任何级别SAEs和导致停药的AEs发生率分别为41.7%、23.9%和9.2%。但值得注意的是,该研究仅纳入接受过1~3线治疗的患者,且MIRV组无铂间期(PFI)≤3个月的患者只占38.8%。同时,靶向人钙黏蛋白-6(CDH6)、间皮素(MSLN)、人类表皮生长因子受体2(HER2)等靶点的ADC也显示出令人鼓舞的前景,值得期待。
尽管多种新型疗法PROC治疗领域取得了一定进展,但由于卵巢癌具有高度异质性,目前仍缺乏有效的药物筛选手段,PROC患者的疗效获益仍有待提升。展望未来,应通过研发新型药物、优化联合治疗策略、探索有效的生物标志物等,进一步优化PROC的治疗策略。首先,应积极探索PROC新药或新型联合治疗策略,包括不同的免疫联合治疗、新型ADC、细胞治疗(如CAR-T治疗、TIL疗法)等,从而突破现有的疗效瓶颈,为PROC带来更加高效的治疗选择。此外,鉴于PD-L1等传统免疫疗效标志物在PROC中的疗效预测价值有限,未来亟需探索更具价值的疗效预测生物标志物。通过精准筛选优势人群,为患者个体化制定治疗策略,可能是改善PROC患者预后的关键。

*转载自医脉通

